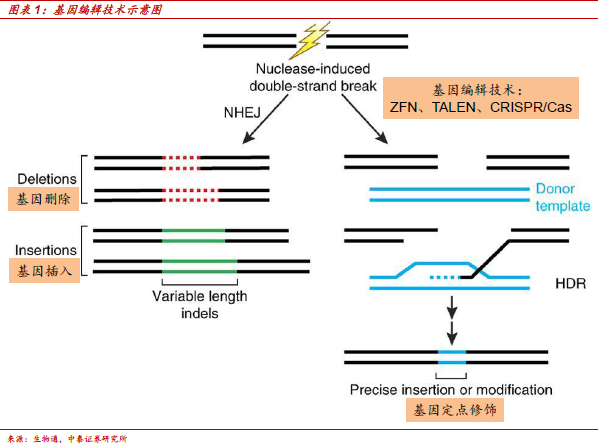
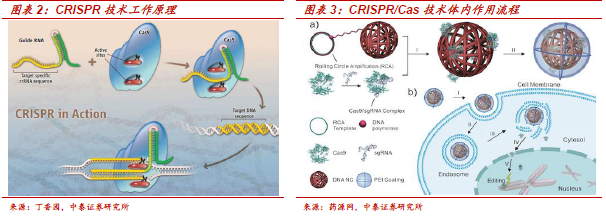
基因編輯CRISPR技術:劃時代的 “上帝之手”,攻克癌癥等難治病。(1)第三代基因編輯技術CRISPR是來自細菌的天然基因編輯工具,可高效精確地插入、剪切和改寫基因;與第一代ZFN和第二代TALEN技術相比,具備低脫靶率、高效(剪切效率是TALEN的100倍)、經濟實惠(從5000美元降低到30美元)、應用范圍廣(全部基因組)等明顯優勢,是基因編輯領域突破性的進展。(2)由于其突破性的技術進展,CRISPR技術目前已研究應用于遺傳缺陷、癌癥、艾滋病等難治病領域,并取得多項驚人成果,未來想象空間無限大。(3)完善的工具庫+技術不斷進步+排他性授權等幾大因素構成的高效生態系統將促進領域爆發式發展。(4)商業化成功,Intellia Therapeutics、Editas Medicine和CRISPR Therapeutics等基因編輯公司專注于CAR-T療法和免疫缺陷病。從技術難度和產業趨勢預判,模式小鼠-腫瘤-遺傳缺陷病-其他疾病是CRISPR落地步驟。其中,二代TALEN應用于CAR-T已有臨床基礎且CAR-T公司與CRISPR公司合作成為趨勢,因此我們判斷三代CRISPR借助技術替代趨勢也將最早落地CAR-T領域。
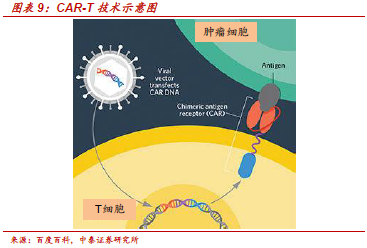
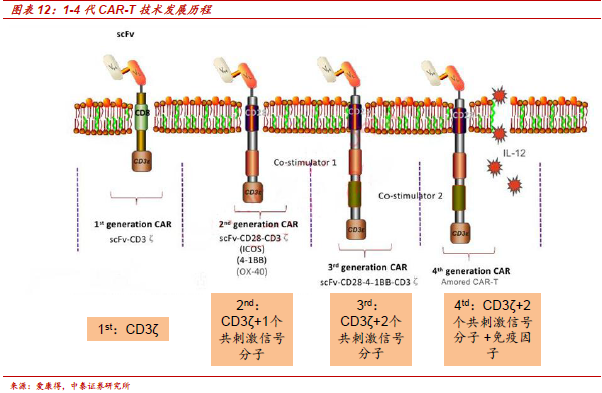
CAR-T:CRISPR技術最早落地領域,CRISPR助力CAR-T 2.0升級版。CAR-T是目前療效最顯著的腫瘤細胞療法,通過不斷增加CAR元件的胞內信號分子數目已發展至第四代,與傳統非特異性的DC細胞療法等相比具備特異性強、療效顯著、副作用低的優點,在血液癌中療效顯著。諾華和JUNO的拳頭產品在淋巴性白血病上均達到90%以上臨床緩解率。但我們認為目前的CAR-T療法只能稱之為1.0版本,因為這些改進都無法解決CAR-T療法存在的副作用(細胞因子釋放綜合征、脫靶毒性)以及應用難點(實體瘤治療效果較差、無法現貨供應)。而CRISPR技術突破性的進展使得其可高效多點地定向編輯T細胞,有效解決現有CAR-T療法的副作用劇烈、實體瘤效果較差、個體療效差異大以及難商業化等問題,助力CAR-T 2.0升級版,CRISPR技術應用到CAR-T療法成為必然。我們判斷,結合CRISPR技術的CAR-T療法將成為下一代CAR-T療法的主流發展方向,有望迅速推進臨床試驗并實現工業化生產。