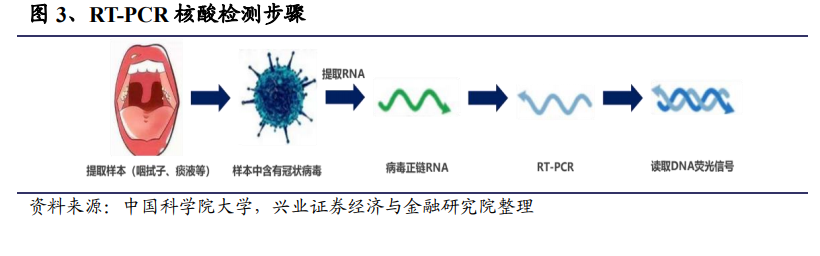
新型冠狀病毒常用的核酸診斷方法有兩種:病毒核酸特異基因檢測和病毒基因組測序。最常見的檢測新型冠狀病毒特異性核酸序列的方法是熒光定量 PCR(聚合酶鏈式反應)。由于新型冠狀病毒是 RNA 病毒,試劑盒檢測基本都采用反轉錄加實時聚合酶鏈式反應法(RT-PCR),擴增病原體的核酸 (RNA) ,同時通過熒光探針實時檢測擴增產物。在 PCR 反應體系中,包含一對特異性引物以及一個Taqman 探針,該探針為一段特異性寡核苷酸序列,兩端分別標記了報告熒光基團和淬滅熒光基團。探針完整時,報告基團發射的熒光信號被淬滅基團吸收;如反應體系存在靶序列,PCR 反應時探針與模板結合,DNA 聚合酶沿模板利用酶的外切酶活性將探針酶切降解,報告基團與淬滅基團分離,發出熒光。每擴增一條 DNA鏈,就有一個熒光分子產生。熒光定量 PCR 儀能夠監測出熒光到達預先設定閾值的循環數(Ct 值)與病毒核酸濃度有關,病毒核酸濃度越高,Ct 值越小。不同生產企業的產品會依據自身產品的性能確定本產品的陽性判斷值。
由于每個 RT-PCR 反應需要 2 個小時左右才出結果,因此,試劑盒在開發時一般都針對病毒序列中高度保守的 2-3 個序列比如編碼 replicase(復制酶)或者necleocapsid(核蛋白衣,核鞘)的核酸序列設計引物,但是各個方法用的序列都不完全相同。一些方法使用 multiplex,也就是把多個目標序列在同一反應管中擴增;另一些采用分步,先用一個目標序列篩查,陽性后再用另一個序列確認,這樣可以有效縮短整個流程時間,加快檢測速度。另外 RNA 病毒變異很快,用多個保守目標序列可以防止病毒變異造成的假陰性。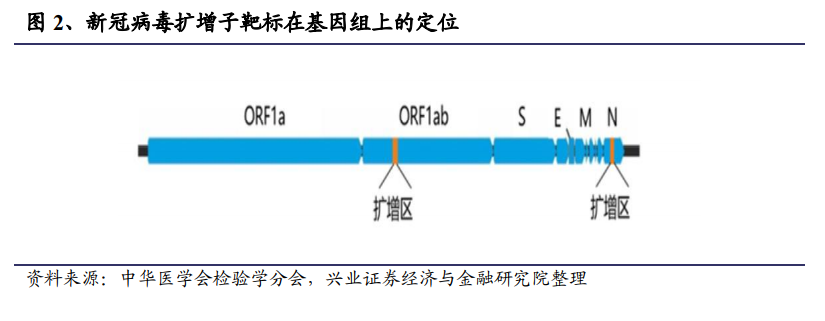
目前批準產品均基于新型冠狀病毒基因組中開放讀碼框 1a/b(open reading frame1ab,ORF1ab)、包膜蛋白(Envelope protein,E)和核衣殼蛋白(nucleocapsid protein,N)進行選擇。不同產品的檢測原理基本一致,但是其引物、探針設計存在不同,有單靶區段(ORF1ab)、雙靶區段(ORF1ab、N 蛋白)、三靶區段(ORF1ab、N 蛋白和 E 蛋白)的檢測和判讀差別。一般檢測位于病毒 ORF1ab 和 N 基因上的兩個靶標,同一份標本需滿足雙靶標陽性或重復檢測為單靶標陽性或兩種標本同時滿足單靶標才能確認 SARS-CoV-2 病毒核酸陽性。