醫藥外包是指將醫藥企業將藥品研發、生產、銷售等環節通過外包的方式交由專業化的企業進行操作。醫藥外包企業按照各自運營的環節大致可以分為CRO(醫藥研發外包組織,Contract Research Organization)、CMO(醫藥定制研發外包組織,Contract Manufacture Organization)、CSO(醫藥銷售組織,Contract Sales Organization)三種。本文中所指醫藥外包主要指CRO和CMO。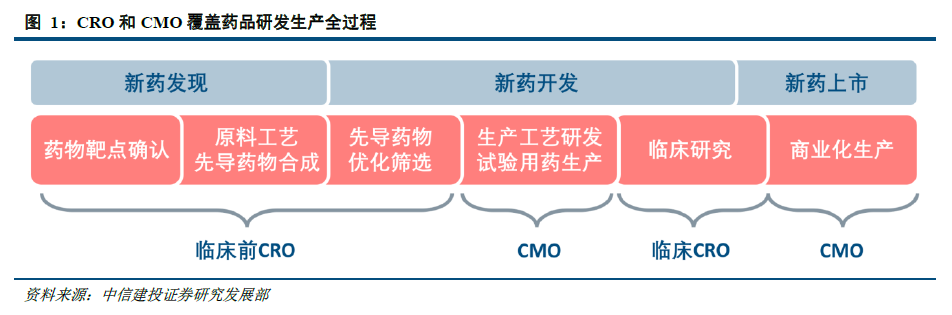
CRO是以合同外包的方式進行藥物開發中早期發現、臨床前研究、臨床試驗等過程的服務的企業。CRO最初誕生于20世紀70年代末期的美國,80年代初FDA對新藥注冊制度不斷完善和嚴格,醫藥企業在研發階段投入的成本和時間都不斷增加,基于成本考慮部分企業開始選擇將某些研發環節外包給CRO。后期,在全球一體化進程不斷深入、醫藥科技迅猛發展的推動下,CRO在美國、歐洲和日本地區迅速發展。CRO的最初原型是數據處理和統計咨詢公司,隨著研發需求不斷擴大,CRO服務范圍也逐漸擴大,不僅僅是臨床試驗和數據處理分析,還包含了藥物發現、臨床前研究、臨床試驗各期研究、新藥研發注冊咨詢等業務。發展至今,CRO為醫藥企業提供研發過程中覆蓋各個環節的服務。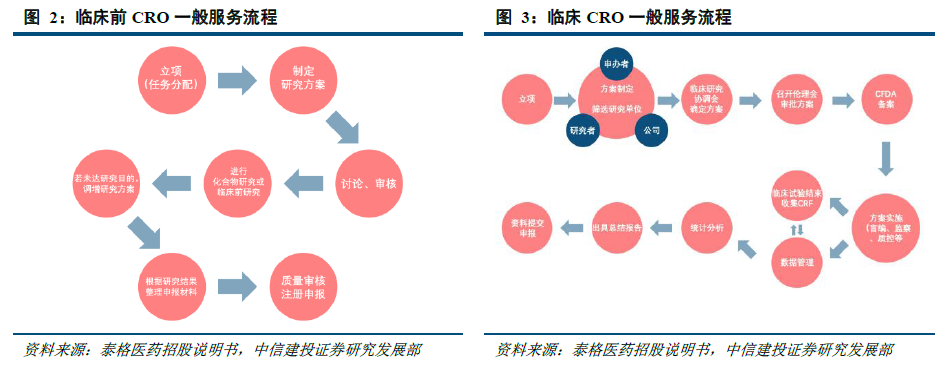
CRO的工作可以覆蓋新藥研發及試驗的各個環節,按照覆蓋的藥物研發環節的不同,CRO又可以分為臨床前CRO和臨床CRO。臨床前CRO主要是在實驗室條件下,通過對化合物研究階段獲得的候選藥物分別進行實驗室研究和活體動物研究,以觀察化合物對目標疾病的生物活性,并對其進行安全性評估的研究活動。臨床前CRO主要業務包括藥效學研究、毒理學研究和動物藥代動力學研究等。另外,對于藥物的臨床前研究,還包括對藥物的合成工藝、提取方法、理化性質及純度、劑型選擇、處方篩選、制備工藝、檢驗方法、質量指標、穩定性、藥理、毒理、動物藥代動力學研究等。而相對而言,臨床CRO則是對于藥物各期臨床試驗環節的外包服務。臨床CRO一般針對藥物臨床試驗,包括I-IV期的臨床試驗以及BE試驗等提供臨床試驗技術服務、現場管理、數據管理和統計分析等,同時也包括提供注冊及申報服務等。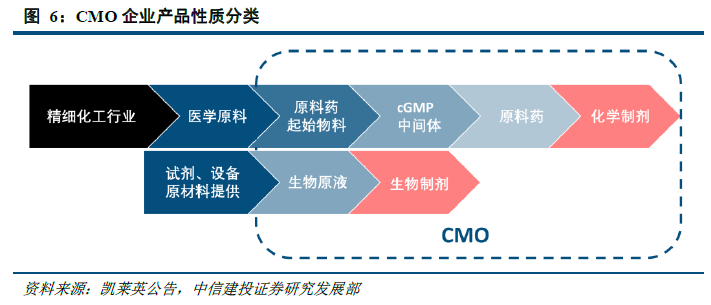
醫藥CRO公司上游為試驗勞務、動物及試劑供應的企業,下游主要服務于制藥企業。臨床試驗CRO企業的產業鏈上游主要是臨床研究服務所需的各類專業人員的勞務供應、實驗動物和試劑供應。臨床試驗機構及研究者往往需要專業的臨床試驗操作。同時作為服務型行業,臨床試驗CRO行業的下游為其研究服務的最終消費者,即國內外化學制藥、生物制藥、醫療器械制造企業、以及部分開展臨床試驗科研項目的醫院。
CMO指的是接受制藥公司的委托,提供醫藥產品生產外包服務的公司。CMO覆蓋的業務包括藥品工藝開發、配方開發、臨床試驗用藥生產、化學或生物合成的原料藥生產、中間體制造、制劑生產(如粉劑、針劑)以及包裝等服務。制藥行業的一系列新形勢——制藥公司及生物技術公司專注于復雜疾病領域、疾病控制出現新趨勢、新興市場不斷崛起以及現有產品配方改造等,拓寬了CMO的市場領域,其生產類別已擴展至固體制劑、液體和半固體制劑以及注射劑等。