FDA 對新型煙草產品的監管態度決定 IQOS 能夠進入美國市場。2019 年,FDA 對新型煙草監管趨嚴,據我們統計,在 IQOS 獲批之前的 4 個月內,FDA 就吸煙對健康的影響以及電子煙對青少年的危害等問題發起的宣傳資料、科學研究、政策監管多達 18 次。在政策明顯趨嚴的背景下,IQOS進入美國市場卻順利獲批,我們認為核心原因有二:1)FDA 對于 IQOS相較于傳統煙草能夠減少對人體的傷害是持認可態度的。FDA 認為 IQOS釋放的有毒化學物質低于吸食傳統煙草。例如丙烯醛的釋放可以減少89%-95%,甲醛釋放可以降低 66%-91%。2)FDA 認為 IQOS 的目標受眾是成年吸煙者,誘導未成年人吸煙概率較低。FDA 認為對于新型煙草產品的監管目的不在于將這一新生事物扼殺,而在于在實現減少對成年人健康影響的同時,最大可能地降低未成年人通過新型煙草接觸尼古丁的風險。換而言之,FDA 認為新型煙草產品應當實現減少已吸煙者健康傷害與不能誘導不吸煙者接觸尼古丁的平衡。在 2018 年 IQOS 的減害煙草制品(MRTP)認證委員會會議中,委員會成員的投票結果表明 IQOS 產品吸引青少年和非煙民接觸尼古丁的可能性較低。吸引已戒煙煙民復吸的可能性也較低。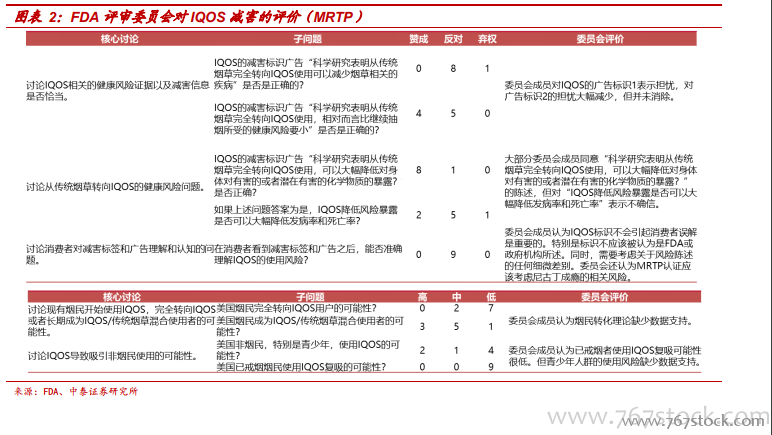
IQOS 正由“爆發式”增長轉向“高速”增長。從 IQOS 上市后的市場表現看,經歷了日本市場 2016-2017 年的爆發式增長后,IQOS 增速正在向高速成長階段邁進。2019Q1 IQOS 煙彈終端銷售量同比增長 35%,與菲莫國際所述“2021 年實現全球煙彈出貨量 900-1000 億支”的目標復合增速基本一致。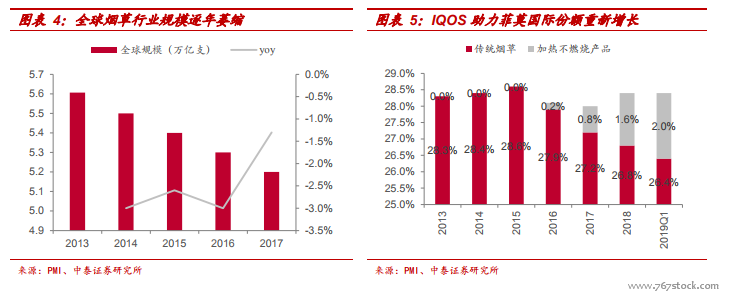
煙民人數突破千萬,IQOS 再現里程碑。2019Q1,IQOS 全球用戶數量達到 1040 萬人(其中包括 730 萬已戒除傳統煙草的用戶),首次突破 1000萬人。按照 PMI 的長期規劃,2025 年全球(不含美國)IQOS 用戶數 4000萬人的目標,尚有 3 倍成長空間