國內核藥可及性和滲透率較低,空間巨大。核醫藥發展已有 100 多年,我國從 20 世紀 50 年代開始研究,起步較晚,落后于發達國家。截至 2020 年 7 月,FDA 共批準了 52 種核藥,其中多種產品在我國并無企業獲批。整體而言,國內核藥的品種數量有待提高,國內研發實力也與發達國家存在一定差距。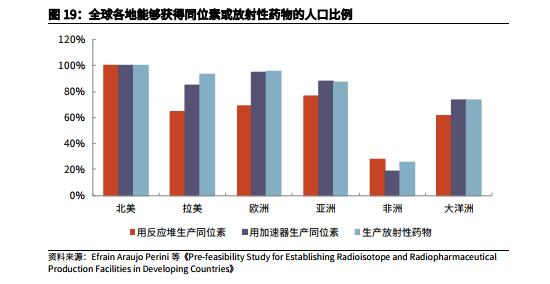
核醫學的快速發展拉動核藥高速放量。近年來,中國的核醫學快速發展,核醫學科建設取得了長足的進步。截至 2019年 12 月 31 日,全國從事核醫學專業相關的科(室)達到 1148 個,相比 2017年增加 23.8%;共有 12578 人從事核醫學相關工作,相比 2017 年增加 38.4%。核醫學科室和人員的增長有力地拉動了核醫藥在臨床上滲透率的迅速提升。從長期來看,全國影像醫學與核醫學專業的研究生導師和在讀研究生人數也呈現明顯的增長態勢,將為我國的核醫藥行業輸送源源不斷的人才,利好行業的長遠發展。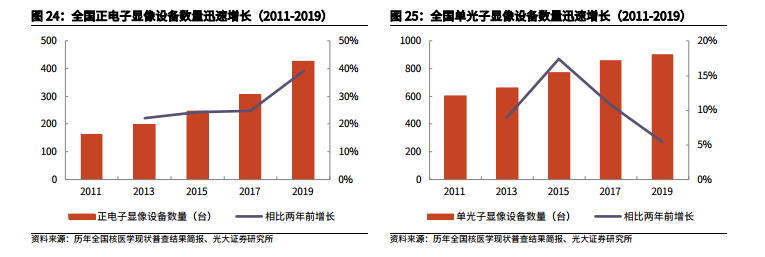
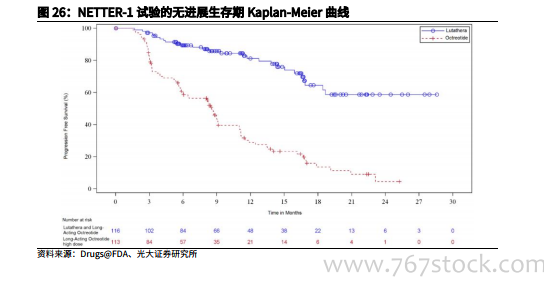
Lutathera:核創新藥的先驅。Advanced Accelerator Applications 公 司 ( 以 下 簡 稱 “AAA” ) 研 發 的Lutathera(lutetium Lu 177 dotatate)于 2018 年獲 FDA 批準上市。Lutathera是一種放射性標記的生長抑素類似物,可用于治療生長抑素受體陽性的胃腸道胰腺神經內分泌腫瘤(GEP-NETs),包括成人前腸,中腸和后腸神經內分泌腫瘤。Lutathera 與生長抑素受體結合,對亞型 2 受體(SSRT2)具有最高的親和力。與表達生長抑素受體的細胞(包括惡性腫瘤)結合后進入細胞內。Lu 177 的 β射線通過在陽性細胞和鄰近細胞中形成自由基來誘導細胞損傷。