ADC 藥物集靶向性和殺傷性于一身,精確制導的“魔法子彈”威力凸顯。ADC(Antibody-drug conjugates)即抗體偶聯藥物,是指將有生物活性的小分子藥物通過連接子連接單克隆抗體,從而精準定位腫瘤細胞釋放高效細胞毒性。相較于其他化療藥物,ADC 藥物通過抗原抗體特異性結合的方式大大提高了給藥特異性,抗體與腫瘤細胞膜上的特異性抗原結合,誘發胞吞作用,使抗體連同其上連接的細胞毒小分子進入細胞,隨后經過溶酶體降解,小分子藥物釋放進入細胞并通過 DNA 插入或抑制微管合成等方式誘導細胞凋亡。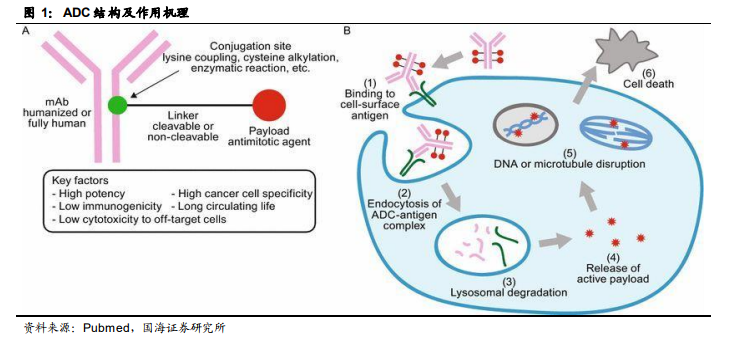
ADC 共經歷了三代技術變革,治療窗口得到較大改善。第一代 ADC 的小分子毒性不夠強,ADC 不夠穩定,大多以失敗告終;第二代藥物采用毒性更強大的小分子,克服了第一代效力不足的弱點,并對抗體進行了優化,但仍采用傳統化學方式偶聯,抗體偶聯比(DAR)均一性差(0-8 個甚至更高)且接頭穩定性不佳,容易在血液中裂解造成嚴重毒副作用,目前共有兩個第二代 ADC 藥物獲批上市;第三代 ADC 藥物的誕生主要得益于定點偶聯技術的發展,如 ThioBridge 技術、非天然氨基酸偶聯、酶促偶聯等,定點偶聯技術解決了抗體歐聯比(DAR)均一性差的老問題,使得藥物在體內分布、代謝和排泄等復雜問題變得簡單,此外一些新型的毒性小分子如 PBD、SN-38 等也被逐漸用于偶聯抗體,ADC 藥物迎來大發展。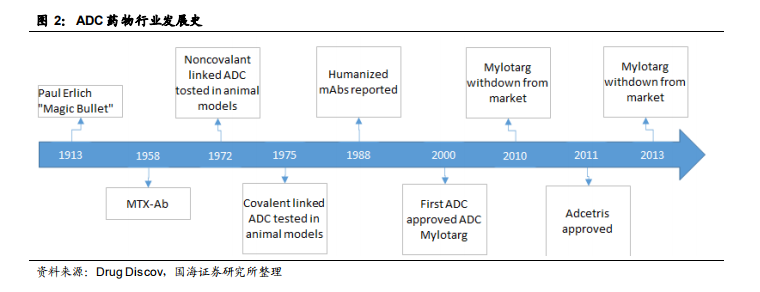
ADC 藥物經過多年發展終于邁向收獲期,精確制導的“魔法子彈”威力凸顯。首先隨著 ADC 技術的迭代和成熟,ADC 治療窗口變大,越來越多已上市或在研的 ADC 藥物展現出的臨床數據非常優異,尤其在過往難治腫瘤或者腫瘤末線治療方面仍有明顯療效:如阿斯利康 2019 年上市的 Enhertu 在晚期 HER2 陽性轉移性乳腺癌方面的應用(DESTINY-Breast01 研究);Immunomedics 的 Trodelvy在治療三陰性乳腺癌方面的突破;GSK 的 Blenrep 在末線治療多發性骨髓瘤患者的優異療效(DREAMM-2 研究)。