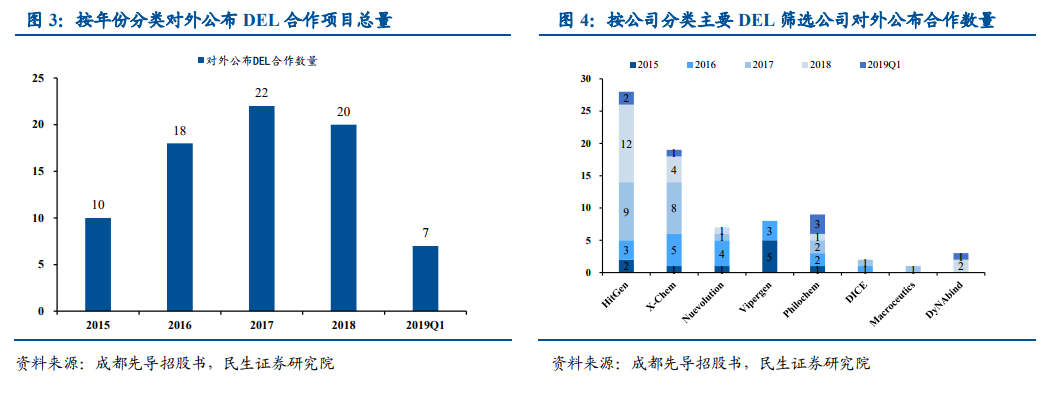
DEL 龍頭公司上市及收購事件吸引投資者關注。DNA 編碼化合物庫(DEL)藥物篩選技術創新性的將低成本大容量化合物庫用于創新藥物篩選,為創新藥的研發尤其是傳統篩選技術不適用的難成藥性靶點的藥物篩選提供新的助力。伴隨著 2019 年 DEL 藥物篩選相關行業兩大重磅事件——安進收購丹麥 DEL 公司 Nuevolution 以及國內 DEL 領域引領者成都先導申報科創板上市相繼披露,DEL 化合物庫篩選先導化合物的技術逐漸引起投資者關注。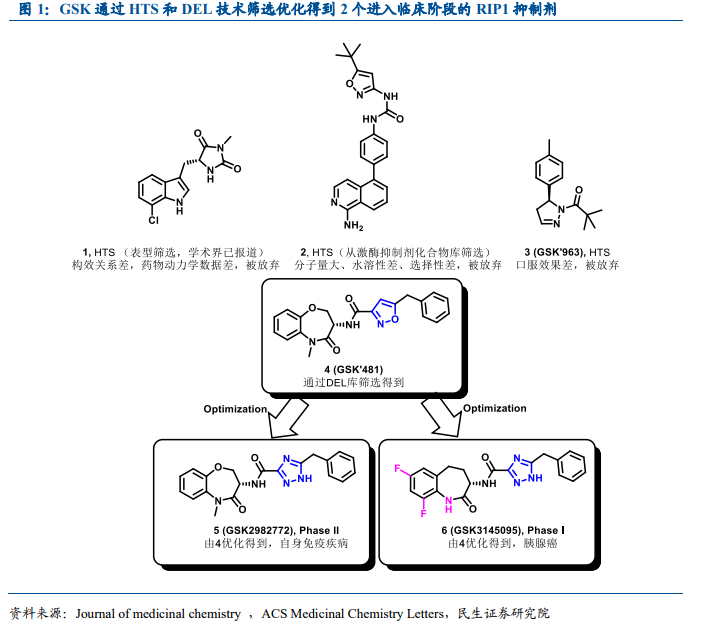
我們發現現在藥物篩選平臺有兩種變現模式,一種是高溢價服務變現(通過具有強 IP 屬性創新性的高溢價服務換取收入,此處突出高溢價是因為有別于傳統 CRO 外包服務商的弱 IP低溢價的跟隨性服務),另一種是產品變現(通過將藥物篩選平臺篩選優化得到的藥物推向上市而換取收入),對比其他藥物篩選技術平臺的變現方式,究竟 DEL 平臺在哪種模式下發展空間更大其實已有定論。我們希望通過將 DEL 篩選技術與常用的先導化合物篩選技術做對比、分析國內外 DEL 技術藥物篩選成功案例和 DEL 領域主要布局企業,對未來 DEL 領域可能發展模式進行了研判,討論分析該技術領域的投資機會。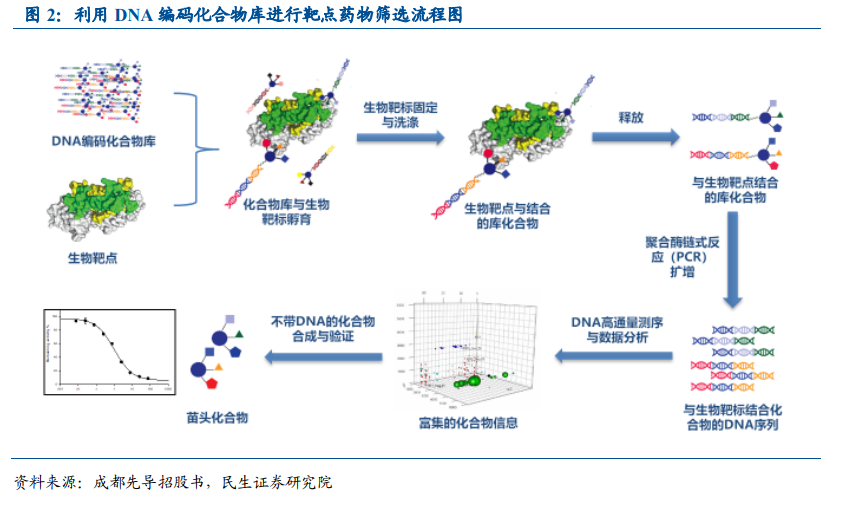
首個進入臨床的 RIP1 的抑制劑歷程:從晶體結構確認到 HTS 篩選失敗。我們通過對第一個成功進入臨床的 RIP1 抑制劑 GSK2982772 發現過程進行梳理,為大家展示 DEL 平臺在創新藥物篩選中的應用實例。RIP1 蛋白是一種程序性壞死作用的關鍵調控蛋白,研究這類蛋白抑制劑最早且最具影響力的團隊為哈佛大學醫學院袁鈞瑛教授,袁教授團隊為第一個發現并定義了 Necropotosis(程序性壞死)這一細胞死亡模式的團隊,并在隨后的研究中通過高通量細胞表型的篩選對 RIP1 抑制劑(當時 RIP1 的晶體結構并未被解析出來)進行研究。袁教授最早針對 RIP1 抑制劑發現文獻報道是在 2005 年,經歷多次優化后拿到了活性最好的小分子抑制劑 Nec-1。但是可惜的是由于藥代動力學數據較差最終未能進入臨床。2013 年清華大學施一公教授團隊成功解析了 RIP1 晶體結構,直接加速了 RIP1 抑制劑開發進程。