FDA 對新型煙草產品的監管態度決定 IQOS 能夠進入美國市場。2019 年,FDA 對新型煙草監管趨嚴,據我們統計,在 IQOS 獲批之前的 4 個月內,FDA 就吸煙對健康的影響以及電子煙對青少年的危害等問題發起的宣傳資料、科學研究、政策監管多達 18 次。在政策明顯趨嚴的背景下,IQOS進入美國市場卻順利獲批,我們認為核心原因有二:1)FDA 對于 IQOS相較于傳統煙草能夠減少對人體的傷害是持認可態度的。FDA 認為 IQOS釋放的有毒化學物質低于吸食傳統煙草。例如丙烯醛的釋放可以減少89%-95%,甲醛釋放可以降低 66%-91%。2)FDA 認為 IQOS 的目標受眾是成年吸煙者,誘導未成年人吸煙概率較低。FDA 認為對于新型煙草產品的監管目的不在于將這一新生事物扼殺,而在于在實現減少對成年人健康影響的同時,最大可能地降低未成年人通過新型煙草接觸尼古丁的風險。換而言之,FDA 認為新型煙草產品應當實現減少已吸煙者健康傷害與不能誘導不吸煙者接觸尼古丁的平衡。在 2018 年 IQOS 的減害煙草制品(MRTP)認證委員會會議中,委員會成員的投票結果表明 IQOS 產品吸引青少年和非煙民接觸尼古丁的可能性較低。吸引已戒煙煙民復吸的可能性也較低。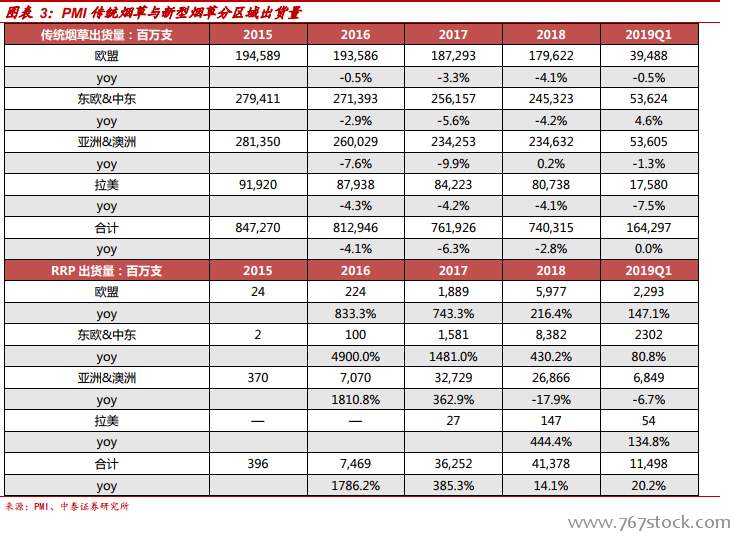
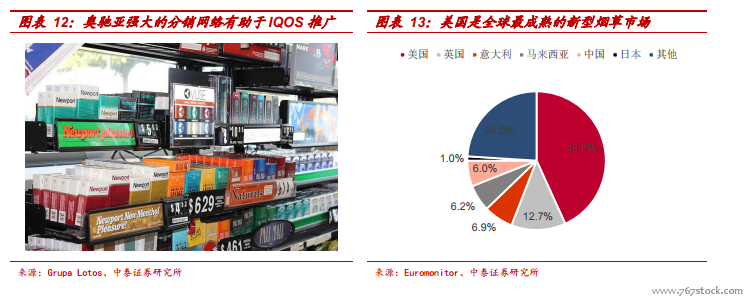
IQOS 是傳統煙草行業萎縮背景下,菲莫國際的必選突圍策略。從 2014年開始,全球卷煙行業在健康意識、控煙政策和稅收政策的合力影響下持續下滑。全球煙草出貨量年復合增速為-2.5%,并且預計每年會繼續以 2%-3%的速度下滑。
美國市場復制日本的成功尚需時日。在先前報告中,我們曾經判斷基于美國市場上述天然優勢,IQOS 上市之后應能取得優于全球市場平均水平的表現。但若要再現日本市場的表現,尚需時間檢驗。1)美國地理上幅員遼闊,不如人口密集的日本市場易于建立口碑相傳的推廣效應。2)日本市場天然沒有煙油式電子煙,競爭格局清晰。而美國市場的加熱不燃燒產品尚需時日樹立口碑。