液流電池是一種液相電化學儲能裝置,其活性物質完全溶解在電解液中,通過活性元素的氧化價態變化來實現能量的存儲與釋放,屬于一種氧化還原電池。一般來說,液流電池需要兩組氧化還原電對來構成正負極,隨著電池的充放電過程,正負極活性元素的氧化價態(電位)發生相應變化。以早期最經典、研究最廣泛的 Fe-Cr 雙液流電池為例,其工作電對為 Fe2+/3+/Cr2+/3+,正極活性物質為 FeCl2,負極活性物質為 CrCl3,電解液基質為鹽酸,正負極間用質子傳導膜進行隔離(避免正負極活性物質直接接觸而發生自氧化還原反應)。電池在滿充狀態下放電時,正極活性物質發生還原反應:Cr3+ + e → Cr2+,負極活性物質發生氧化反應:Fe2+ → Fe3+ + e,整體可合并為:Cr3+ + Fe2+ → Cr2+ + Fe3+,即三價 Cr離子對二價 Fe 離子的氧化及自身的還原過程,電子從負極出發,經外電路后到達正極。充電儲能的過程則與之相反。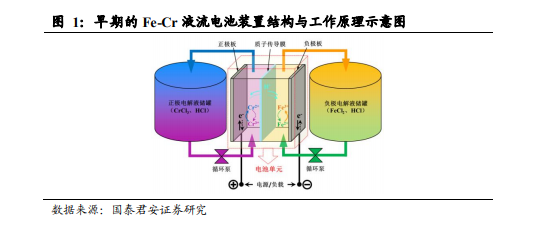
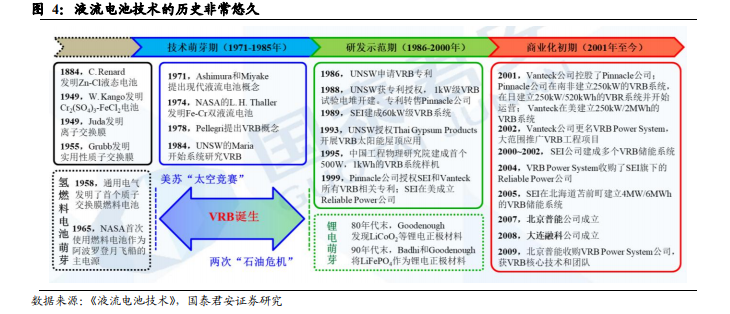
液流電池技術的起源非常悠久,跨越一個多世紀。最早可追溯到 1884年,法國工程師 Charles Renard 發明的鋅-氯液態電池,被用作軍用飛艇螺旋槳的動力源,續航時間 23 分鐘,往返飛行里程 8 公里,電池整體重 435kg,以三氧化鉻和濃鹽酸為氯源。該電池與今天的鋅-溴液流電池
相似(但沒有附加的流體驅動系統),在當時作為一次電池使用,沒有明顯競爭力,隨后銷聲匿跡。半個多世紀后的 1949 年,德國科學家 WalterKango 發明了“液態儲存電池”,并申請了正式專利,該電池以硫酸鉻氯化亞鐵為工作物質且存放在獨立容器中,以硫酸為基質,石墨為惰性
電極,該專利被視為歷史上液流電池的首個專利。此后,Kango 進一步篩選出 6 組可用于構建液態電池的電對,以氯化鈦、氯化鐵、硫酸鉻等過渡金屬鹽作為活性物質。這種液態儲存電池的裝置結構已初具現代液流電池的雛形,但設計簡陋,且循環性能較差,主要是由于正負極金屬
離子交叉污染引起的自放電很嚴重,導致電壓失穩和容量快速衰減,且所用原物料的腐蝕性往往很強或具有高毒性,在成本上也不具備顯著優勢,因此基本不具有商業化價值。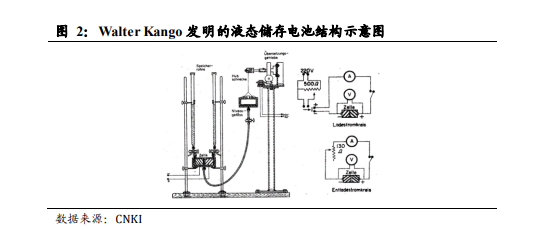
現代液流電池技術的進步與離子交換膜技術的發展密切相關。1950 年左右,膜技術取得突破,人們獲得了具有選擇透性的離子交換膜,為現代版液流電池技術的發展奠定了基礎。1955 年,通用電器公司將聚苯乙烯磺化修飾后得到了第一個質子交換膜(Proton Exchange Membrane,PEM),并將其作為燃料電池的電堆隔膜。PEM 只允許質子通過,阻斷其他離子透過,因此該技術很快被移植到液流電池中,作為正負極隔膜以抑制內部自放電。到了 80 年代,通用公司與杜邦公司合作,依托后者的全氟磺酸樹脂專利技術,開發出了 Nafion 質子交換膜,并被加拿Ballard 公司應用到燃料電池中,使得其性能大大改善。由于全氟磺酸膜的質子傳導性能優異,還具有極強的抗氧化和酸腐蝕性,很快被引入液流電池中,至今仍然是液流電池的主流隔膜材料。